PD-L1获临床试验批件 红日药业毛利率持续下滑
摘要: 近日,红日药业(300026)收到国家药监局下发的临床试验通知书。经国家药监局审查,公司申报的创新药艾姆地芬片符合药物临床试验审评审批的有关要求,获准开展实体肿瘤的临床试验,并将于近期开展临床试验,艾
近日,【红日药业(300026)、股吧】(300026)收到国家药监局下发的临床试验通知书。经国家药监局审查,公司申报的创新药艾姆地芬片符合药物临床试验审评审批的有关要求,获准开展实体肿瘤的临床试验,并将于近期开展临床试验,艾姆地芬片为国内首个获得临床试验批准的口服PD-L1小分子抑制剂。
毛利率持续下滑 政策组合拳走创新道路?
红日药业在产的药品包括成品药、中药配方颗粒、辅料及原料药、医疗器械等。其中中药配方颗粒营收占比最高,2019年上半年实现营业收入为12.39亿元,同比增长25.81%,营收占比为54.15%;其次血必净注射液实现营业收入4.26亿元,同比下降2.76%。
2019年前三季度红日药业实现营业收入36.02亿元,同比增长18.89%;实现归母净利润5.16亿元,同比增长11.45%;经营活动产生的现金流量净额为2.26亿元,同比下降38.42%。
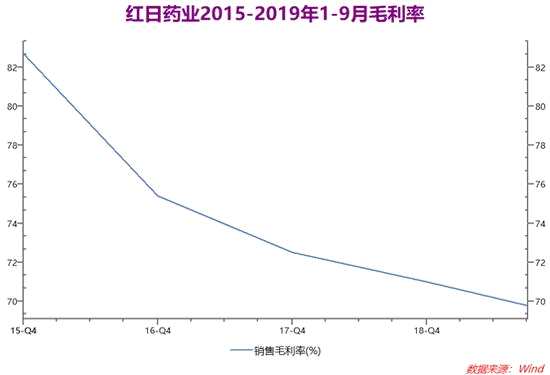
从盈利能力来看,红日药业的销售毛利率处于下降趋势,2019年前三季度毛利率为69.76%,相比2015年前三季度的83.14%有较大降幅。销售费用高企一直是药企的通病,红日药业的销售费用率近年有所下降,但是占营业收入的比例依然接近40%,蚕食了部分毛利。那么销售费用构成如何呢?根据2019年半年报,销售费用中占比前三的分别是调剂服务费、市场调研费和学术推广费。
随着国家医疗卫生体制改革的不断推进与深化,行业政策密集出台,对药品经营环境造成一定的影响,特别是医保控费、公立医院改革、医联体、限制辅助用药、带量采购等政策的实施,二次议价愈演愈烈、GMP 飞行检查、工艺核查、安全环保监管力度加大等影响因素都将对药品生产经营造成直接影响,带来行业竞争的新变革。
国家的一系列措施为创新药提供了诸多利好,国内的药物研发申报数量和上市数量呈现逐步上升趋势。红日药业的创新药艾姆地芬片的临床试验获批展示了公司在创新药上的布局,根据2019年半年报,公司上半年的研发投入为9672.03万元,同比增长22.71%,占营业收入比例为4.23%。截至6月30日,研发管线中包括4个化药1.1类,其中除了甲苯磺酰胺处于申报生产阶段,其他的均处于较早期。
国内首个PD-L1小分子抑制剂
艾姆地芬片为国内首个获得临床试验批准的口服PD-L1小分子抑制剂,与目前已经获得批准上市的同靶点注射用单抗药物相比,具有的优势包括:能够透过细胞膜进入细胞内;在某种程度上可进入脑组织,用于脑部肿瘤的治疗;可口服,患者顺应性强;在生产工艺 、剂型设计和给药方式等多种层面的研究也颇为成熟,成本低;可避免大分子药物能引起的不良反应。
同靶点药物方面,目前国内外尚无已经获得批准上市的PD-L1小分子抑制剂,罗氏子公司基因泰克公司研发的阿特珠单抗(Tecentriq)简称“T药”,是美国FDA批准的首个PD-L1单抗药物,为PD-L1大分子抑制剂。罗氏2018年财报显示,T药的销售额为7.72亿瑞士法郎,同比增长59%。
目前全球有9款PD-1/PD-L1药物获批上市,其中 BMS 的 Opdivo、MSD 的 Keytruda、君实生物的特瑞普利单抗、信迪利单抗和恒瑞的卡瑞利珠单抗等目前已经在国内上市,后续百济神州的 PD-1 也已经提交上市申请。
值得一提的是,10月15日,百济神州自主研发的BTK抑制剂泽布替尼,宣布获得美国FDA加速批准上市,用于治疗既往接受过至少一项疗法的套细胞淋巴瘤患者。成为我国第一款自主研发、在FDA获批的抗癌新药。
医保局成立以来,医保谈判品种将直接实现在各省挂网销售,缩短了创新药放量周期长的问题。众所周知,创新药的研发有着投入大、失败率高的的特点,而艾姆地芬片处于临床试验的早期阶段,后续进展值得关注。
药物,创新